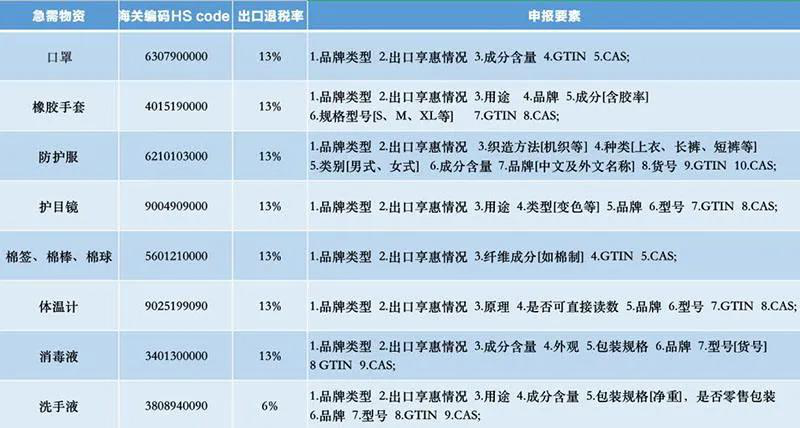
國際上疫情再度爆發(fā),對于防疫物質(zhì)的需求也是與日俱增。近期來咨詢口罩出口的企業(yè)也非常多,今天我們智皓國際就來談?wù)効谡秩绾问浅隹谝约俺隹谛枰南嚓P(guān)資質(zhì)。
首先我們必須知道您出口的口罩種類。 國內(nèi)的口罩分三種:
第一種是醫(yī)用口罩
作為醫(yī)療器械管理的醫(yī)用口罩也分為三種:醫(yī)用防護(hù)口罩、一次性普通醫(yī)用口罩和醫(yī)用外科口罩。 生產(chǎn)醫(yī)用口罩,需要向省級食品藥品監(jiān)督管理局器械處申請辦理”醫(yī)療器械產(chǎn)品注冊證“、”醫(yī)療器械生產(chǎn)許可證“。而且還需要10萬級以上的潔凈車間,并具備微生物試驗?zāi)芰拖嚓P(guān)理化試驗?zāi)芰ΑK^十萬級凈化車間就是指空氣潔凈度為十萬級的潔凈車間。空氣潔凈度是指潔凈環(huán)境中空氣含懸浮粒子量的多少的程度,通常空氣中含塵濃度高則空氣潔凈度低,含塵濃度低則空氣潔凈度高。也就是以每立方米空氣中的最大允許粒子數(shù)來確定其空氣潔凈度等級。
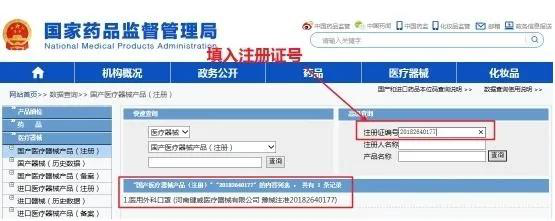
登錄“國家藥品監(jiān)督管理局”(www.nmpa.gov.cn)的官網(wǎng),然后點擊“醫(yī)療器械”-“國產(chǎn)器械”的欄目。根據(jù)頁面指示,輸入該款口罩的醫(yī)療器械注冊證號或企業(yè)名稱等,就可以知道與產(chǎn)品相關(guān)的企業(yè)生產(chǎn)信息,批準(zhǔn)文號信息,即可知道是否合格。
第二種是勞保口罩

勞保口罩也叫 特種勞動防護(hù)用品 ,生產(chǎn)此類產(chǎn)品需要向省級技術(shù)監(jiān)督局申請 工業(yè)品生產(chǎn)許可證 ,并向國家安全生產(chǎn)監(jiān)督管理總局申請 “特種勞動防護(hù)用品安全標(biāo)志”認(rèn)證 ,簡稱為“LA”認(rèn)證。
以上兩種口罩申報出口時,需要提供以下資料:
1: 營業(yè)執(zhí)照
2:企業(yè)生產(chǎn)許可證
3:產(chǎn)品檢驗報告
4:醫(yī)療器械注冊證
5:產(chǎn)品說明書、標(biāo)簽
6:產(chǎn)品批次/號
7:產(chǎn)品質(zhì)量安全書
8:產(chǎn)品樣品圖片及外包裝圖片
第三種是日常防護(hù)口罩

日常防護(hù)口罩相對簡單,不用辦理任何許可證照,將產(chǎn)品向有資質(zhì)第三方檢測機(jī)構(gòu)按照相應(yīng)標(biāo)準(zhǔn)送檢, 取得國家權(quán)威檢測報告,具備CMA、CNAS認(rèn)可標(biāo)識 ,即可上市銷售。
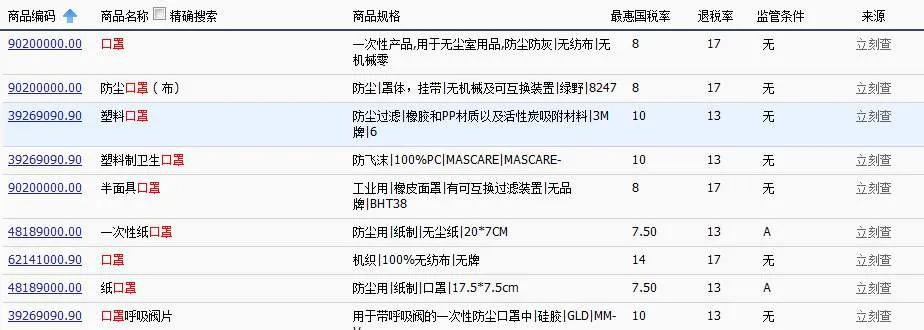
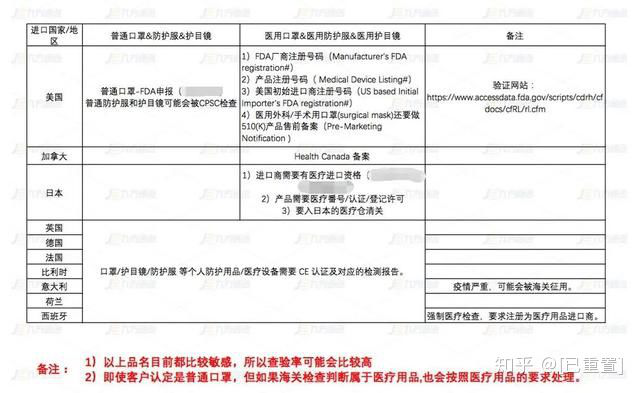
我國海關(guān)對口罩出口沒有限制,資質(zhì)齊全的企業(yè)和合規(guī)的產(chǎn)品可以放心大膽地正常申報,關(guān)鍵是出貨以前確認(rèn)國外的清關(guān)要求。 根據(jù)《醫(yī)療器械監(jiān)督管理條例(2017修正)》第四十四條:出口醫(yī)療器械的企業(yè)應(yīng)當(dāng)保證其出口的醫(yī)療器械符合進(jìn)口國(地區(qū))的要求。 口罩在不同的國家有不同準(zhǔn)入門檻及要求,作為出口企業(yè)必須要了解:
如美國對于醫(yī)用口罩的管理機(jī)構(gòu)是美國食品藥品監(jiān)督管理局(FDA), 出口到美國的口罩若需要銷售,必須要拿到美國食品藥品監(jiān)督管理局(FDA)認(rèn)證 才可以在美國本土市場進(jìn)行銷售活動。在歐盟,口罩屬于PPE個人防護(hù)用品,“危及健康的物質(zhì)和混合物”。 根據(jù)歐盟新法規(guī),所有出口歐盟的口罩必須獲得CE認(rèn)證證書。 帶有CE認(rèn)證標(biāo)志的口罩是歐洲經(jīng)濟(jì)區(qū)批準(zhǔn)的用于安全,健康和環(huán)保標(biāo)準(zhǔn)的一次性口罩。就像NIOSH根據(jù)其效率等級將呼吸器分級為N95,N99或N100一樣,CE將其口罩分級為FFP1,F(xiàn)FP2或FFP3。
中國公司口罩出口海外需具備哪些資質(zhì)?
01、用于銷售
需要經(jīng)營范圍內(nèi)有醫(yī)療器械經(jīng)營許可證的,進(jìn)出口權(quán)的,才能出口。
02、用于贈送或代為采購
作為贈送的,或者代關(guān)聯(lián)公司(兄弟公司,母子公司)采購的,要提供采購的廠家或公司的國內(nèi)生產(chǎn)廠家的相關(guān)資質(zhì)證明文件,與我們進(jìn)口時要國外提供三證(營業(yè)執(zhí)照,產(chǎn)品醫(yī)療器械備案證明,廠家檢查報告)一個道理。
重點國家口罩進(jìn)口必備資質(zhì)
美國
01、必要資料(資質(zhì))
提單,箱單,發(fā)票
美國進(jìn)口的口罩,若需要銷售,必須要拿到FDA認(rèn)證才可以在美國本土市場進(jìn)行銷售活動。對于自用和贈送的口罩,大家在出口的時候最好先問一下美國接收方面,是否也需要FDA認(rèn)證,或者采購原本就通過FDA認(rèn)證的口罩進(jìn)行出口。

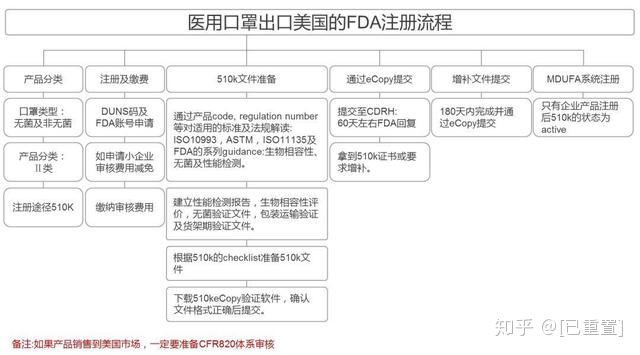
美國口罩分為醫(yī)用口罩和普通防護(hù)口罩。
1.醫(yī)用口罩出口資質(zhì):需要有相關(guān)產(chǎn)品的FDA認(rèn)證(美國食品藥品監(jiān)督管理局)和亞馬遜相關(guān)產(chǎn)品類目的分類審核,才能上架銷售和解決物流清關(guān)問題;FDA認(rèn)證需要每年向美國食品藥品監(jiān)督管理局繳納一定金額的注冊費、年費,收費為5000美元左右。
2.普通防護(hù)口罩出口資質(zhì):不需要FDA認(rèn)證,只需要有口罩類目的分類審核就可以銷售;另外普通防護(hù)口罩的出口需要借助物流商渠道進(jìn)行FDA申報。
02、口罩要求
根據(jù)HHS(美國衛(wèi)生及公共服務(wù)部)法規(guī),NIOSH(美國國家職業(yè)安全衛(wèi)生研究所)將其認(rèn)證的防顆粒物口罩分為9類。具體的認(rèn)證則由NIOSH下屬的NPPTL實驗室操作。
在美國,按過濾網(wǎng)材質(zhì)的最低過濾效率,可將口罩分為三種等級——N ,R ,P。
N類的口罩只能過濾非油性顆粒物,比如:粉塵、酸霧、漆霧、微生物等。空氣污染中的懸浮微粒,也多是非油性的。
R口罩只適合過濾油性顆粒物及非油性顆粒物,但用于油性顆粒物時限制使用時間不得超過8小時。
P類口罩則既可過濾非油性顆粒物,又可過濾油性顆粒物。油性顆粒物比如:油煙、油霧等。
根據(jù)過濾效率的不同,又有90,95,100的差別,分別指在標(biāo)準(zhǔn)規(guī)定的測試條件下最低過濾效率為90%,95%,99.97%。
N95不是特定的產(chǎn)品名稱。只要符合N95標(biāo)準(zhǔn),并且通過NIOSH審查的產(chǎn)品就可以稱為“N95型口罩”。
歐盟
01、必要資料(資質(zhì))
提單,箱單,發(fā)票
02、口罩要求
在歐盟,口罩屬于PPE個人防護(hù)用品,“危及健康的物質(zhì)和混合物”。2019年起,歐盟新法規(guī)PPE Regulation (EU) 2016/425強(qiáng)制執(zhí)行,所有出口歐盟的口罩必須在新法規(guī)的要求下獲得CE認(rèn)證證書。

CE認(rèn)證是歐盟實行的強(qiáng)制性產(chǎn)品安全認(rèn)證制度,目的是為了保障歐盟國家人民的生命財產(chǎn)安全。
日本
01、必要資料(資質(zhì))
提單,箱單,發(fā)票。出口日本的PMDA注冊醫(yī)療器械公司希望把產(chǎn)品投放到日本市場必須要滿足日本的Pharmaceutical and Medical Device Act (PMD Act),在PMD Act的要求下,TOROKU注冊系統(tǒng)要求國外的制造商必須向PMDA注冊制造商信息。
02、口罩要求
包裝上印有ウィルスカット99%的字?樣?都是超過國內(nèi)過濾效率95%(N95口罩)標(biāo)準(zhǔn)的醫(yī)用口罩!
PFE:0.1um微粒子顆粒過濾效率
BFE:細(xì)?菌?過濾率
VFE:病毒過?濾率
ウィルスカット:病毒攔截
00001. 醫(yī)用防護(hù)口罩:符合中國GB 19083-2010 強(qiáng)制性標(biāo)準(zhǔn),過濾效率≥95%(使用非油性顆粒物測試)。
00002. N95口罩:美國NIOSH認(rèn)證,非油性顆粒物過濾效率≥95%。
00003. KN95口罩:符合中國GB 2626 強(qiáng)制性標(biāo)準(zhǔn),非油性顆粒物過濾效率≥95%
注意:需要供應(yīng)商具備二類醫(yī)療器械經(jīng)驗許可憑證,產(chǎn)品需要醫(yī)療番號/認(rèn)證/登記許可證,且還需要入日本的醫(yī)療倉清關(guān),情況特殊復(fù)雜,建議賣家謹(jǐn)慎考慮。
韓國
01、必要資料(資質(zhì))
提單,箱單,發(fā)票,韓國進(jìn)口商營業(yè)執(zhí)照,韓國收貨人需要到韓國藥監(jiān)局Korea Pharmaceutical Traders Association. 提前備案進(jìn)口資質(zhì)(沒有不行)。
網(wǎng)址:www.kpta.or.kr
企業(yè)自用又是受贈的情況,可以自行進(jìn)口,不需要有相關(guān)資質(zhì)。
02、口罩要求
韓國的口罩標(biāo)準(zhǔn)KF (Korean filter) 系列,KF系列標(biāo)準(zhǔn)是由韓國的食品藥品管理部門發(fā)布的韓國主流口罩標(biāo)準(zhǔn) 。KF系列分為KF80、KF94、KF99。KF80:≥80% (僅鹽性介質(zhì)) ;KF94:≥94%(油性和鹽性介質(zhì)) ;KF99:≥99% (油性和鹽性介質(zhì)) 。
口罩還需要有詳細(xì)的原產(chǎn)地標(biāo)識,如果是中國制造務(wù)必有標(biāo)簽:Made in China, 生產(chǎn)廠家信息、保質(zhì)期,還要準(zhǔn)備成分含量說明,制造工藝流程,這些文件都有了還沒有結(jié)束,還需要貨物到了韓國以后進(jìn)行精監(jiān)化驗送交樣品到實驗室,化驗合格后方可進(jìn)入韓國市場銷售流通。
澳大利亞
01、必要資料(資質(zhì))
提單,箱單,發(fā)票
02、口罩要求
AS/NZS 1716:2012是澳大利亞和新西蘭的呼吸保護(hù)裝置標(biāo)準(zhǔn),相關(guān)產(chǎn)品制造流程和測試必須符合本規(guī)范。
該標(biāo)準(zhǔn)規(guī)定了防顆粒口罩制造過程中必須使用的程序和材料,以及確定的測試和性能結(jié)果,以確保其使用安全。
03、個人行郵方式
00001. 由于每個國家關(guān)于進(jìn)口口罩的要求不同,建議大家出口前務(wù)必咨詢當(dāng)?shù)氐拇砉净蛘呓邮辗剑苊馕镔Y被扣或者被退回的問題。
00002. 自用口罩的出口以及快遞,數(shù)量一定要在合理范圍,如果數(shù)量巨大也有可能被國外海關(guān)扣押。
00003. 目前航空海運運力部分暫停,運輸時間都相對較長,建議在發(fā)貨后留意單號更新,同時耐心等待,只要沒有違規(guī)問題,一般不會被扣押或者退回。
再次提醒:
建議中國賣家及時關(guān)注國內(nèi)外防疫物資出口資質(zhì)認(rèn)證和監(jiān)管要求,避免造成產(chǎn)品被扣押和退回的風(fēng)險。屬于醫(yī)療器械類的口罩,不同國家的資質(zhì)和要求都不相同,這點賣家們一定要注意。國內(nèi)外銷售都需要先獲得《第二類醫(yī)療器械經(jīng)營備案憑證》,若想在跨境平臺銷售,除了類目審核,還需要產(chǎn)品認(rèn)證,歐美必須通過當(dāng)?shù)貒艺J(rèn)證許可,如歐盟CE認(rèn)證,美國NIOSH認(rèn)證。歐盟CE認(rèn)證還需要注意包裝、質(zhì)量符合要求,要有歐洲代理信息。并最好保留好認(rèn)證證書,采購發(fā)票或原材料發(fā)票。
沒有一個冬天不可逾越,沒有一個春天不會到來,春暖花開始,山河定無恙!愿早日戰(zhàn)勝疫情。 心有大我,至誠報國。祝愿早日戰(zhàn)勝疫情,明媚的陽光終會照亮這片土地。 愿我們早日能戰(zhàn)勝疫情,摘下口罩去想去的地方,見想見的人。



